2022年我国医疗器械产业发展现状:营业收入预计达1.3万亿元,增速12%左右,显著高于医药工业整体增速
- 18
- 2023-01-15 20:40:03
- 400
炒股就看金麒麟分析师研报,权威,专业,及时,全面,助您挖掘潜力主题机会!
来源:医药经济报
2022年我国医疗器械产业发展现状
2022年,是党和国家事业发展进程中极为重要的一年。百年变局和世纪大疫持续交织,全球医疗卫生事业继续经受考验。我国医疗器械产业稳中求进,逆势前行,在高质量发展道路上保持了创新发展的良好趋势:产业规模持续高增长,发展质量迈向新高度,创新发展迈出新步伐,国际竞争力提升新水平,展现出我国医疗器械产业发展的强大韧性。
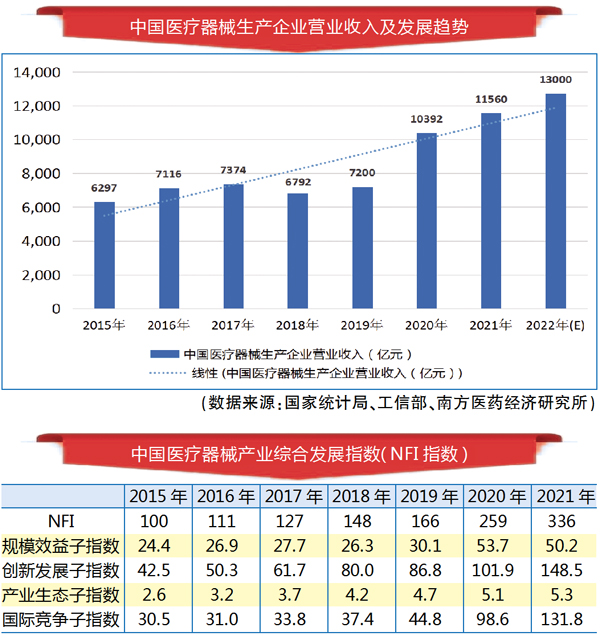
产业规模持续高增长
一是我国医疗器械产业规模持续高增长。据南方所分析,2021年我国医疗器械产业营业收入(规上+规下数据)达1.156万亿元,同比增长为11.24%,从2015年6297亿元增长到2021年11560亿元,年均复合增长率为10.65%,高于我国总体制造业增长水平。2022年我国医疗器械产业营业收入预计达1.3万亿元,增速12%左右,显著高于医药工业整体增速。新冠检测试剂是拉动行业增长的主要力量,我国疫情防控核酸检测常态化,新冠核酸检测试剂和抗原检测试剂大量出口国际市场,促使相关企业业绩大幅增长。此外,医疗新基建和“千县工程”的推进,促进了医疗设备市场扩容和国产替代加速。
二是医疗器械产品首次注册数量稳步发展。境内第三类医疗器械产品首次注册数量大幅增长,连续两年保持两位数的增长,2022年达到1844件,同比增长63.04%。境内第二类医疗器械首次注册数量自2020年突破1万件后,近三年来一直维持在1万件水平左右,远超疫情前的6000件水平,2022年达到13334件。境内第一类医疗器械产品新增备案数量,2022年达到29807件,高于疫情前水平。按细分领域分布来看,2022年境内医疗器械产品首次注册数量较多的为体外诊断试剂、无源植入器械两个领域,分别占比17.2%和21.7%,两者合计占全部产品首次注册数量的38.9%。
三是我国医疗器械生产企业数量突破3万家。近三年,新冠疫情影响下,我国医疗器械生产企业数量增长较快,于2022年突破3万家,截至2022年9月达31503家。从生产医疗器械产品类别来看,可生产一类医疗器械产品的企业数量19025家,快速增长;可生产二类医疗器械产品的企业数量14119家,平稳增长;可生产三类医疗器械产品的企业数量2412家,有较快增长;三者之比约为8:6:1,比值与上一年保持一致。
四是经营企业数量突破110万家。截至2022年9月,我国医疗器械经营企业数量达116万家。近几年来,医疗器械经营企业都以两位数以上的速度增长,2021年突破了100万家,达108万家,同比增长20.88%。医疗器械经营企业规模的不断扩大,也促进了整体产业的蓬勃发展。
发展质量稳步创新高
一是利润总额增长趋缓。2021年,我国医疗器械规模以上生产企业利润总额为1021亿元,与2020年相比略有下降,但与疫情前相比仍有近1倍的大幅增长。2021年,我国医疗器械上市企业营业利润总额为870亿元,同比增长11.36%,与疫情前相比更是有超过2倍的大幅增长。
二是营业利润率较疫情前明显增长。我国规模以上医疗器械生产企业利润率(利润总额÷营业收入),从2015年的9.49%增长到2019年的12.80%,2020年达到17.45%;2021年为15.07%,略有下降,但与疫情前相比仍有较为明显的增长。
三是产业集中度不断增强。我国医疗器械规模以上生产企业营业收入从2015年4241亿元增长至2021年6771亿元,占产业整体营业收入比重达60%左右。2022年,我国医疗器械上市企业数量达163家,同比增长15.60%,此前两年更是以30%高速增长。2021年,我国上市医疗器械企业营业收入达到3324亿元,同比增长18.82%。上市企业营收规模占整体行业规模从2017年的16%增长到2019年的29%,其中前20强上市企业规模占整体行业规模的比重从2017年的7%增长到2021年的16%,两个比重在近五年持续增长。这充分表明头部企业发展态势良好,行业集中度逐年上升,这与《“十四五”医药工业发展规划》提出的“行业龙头企业集中度进一步提高”发展目标相符合。
创新发展迈出新步伐
一是法规标准体系更加完善。加快推进《医疗器械监督管理条例》配套制度建设,出台了《医疗器械生产监督管理办法》《医疗器械经营监督管理办法》等一系列规章制度。标准体系的覆盖面、系统性和国际协调性不断提升,截至2022年12月31日,我国医疗器械标准共计1919项,覆盖了我国医疗器械各专业技术领域,与国际标准一致性程度已达90%。其中,国家标准260项,行业标准1659项;强制性标准284项,推荐性标准1635项。
二是创新医疗器械发展提速。2022年,国家药监局批准创新医疗器械55件,同比增长57.14%。自2014年以来国家药监局共批准创新医疗器械189件,更多的创新高科技医疗器械正快速受惠于民,不断满足人民群众日益增长的健康需求,成为推动产业高质量发展的强大动力。
三是高技术企业新产品开发项目数大幅增长。2021年,我国医疗器械高技术企业新产品开发项目数量为15962件,同比增长28.39%。近三年来,医疗器械高技术产业新产品开发项目均以30%左右的速度大幅增长。
四是研发强度整体呈现稳定且小幅提升趋势。2021年,我国医疗器械上市企业研发强度为6.39%,近几年均保持在6%以上水平;2020年我国医疗器械高技术产业研发强度为3.97%,近几年保持近4%水平,高于整体高技术产业2.5%的平均水平。
国际竞争力提升新水平
一是医疗器械进出口规模稳步提升。2021年,我国医疗器械产品进出口额为8724.39亿元人民币,同比下降24.50%。其中,进口额3243.85亿元人民币,同比增长10.63%,继续保持良好增长态势;随着海外市场对防疫医疗器械产品需求趋向稳定,出口额5480.54亿元人民币,同比下降36.44%,但与疫情之前相比仍有超过75%的大幅增长。截至2022年11月,我国医疗器械进出口额为7438.57亿元人民币。其中,进口额为2996.78亿元人民币,出口额为4441.79亿元人民币。受新冠疫情影响,全球抗击新冠疫情医疗器械产品需求旺盛,我国医疗器械进出口较疫情前整体规模提升了一个台阶。
二是中国稳居全球第二大医疗器械市场。在新冠疫情的刺激下,中国医疗器械市场迅速扩大,在全球医疗器械市场中彰显越来越重要的地位。根据弗若斯特沙利文数据,2021年,全球医疗器械行业市场规模预计达34074亿元,同比增长8.15%。根据南方所数据,2021年,中国医疗器械市场规模约为11560亿元,增速约为全球市场增速的1.5倍,市场份额接近全球市场的三分之一,中国仅次于美国稳居全球第二大医疗器械市场。
三是中国医疗器械企业国际影响力不断扩大。越来越多技术先进、合规运营、质量健全的中国企业正在逐渐展现其国际影响力。根据国外网站Medical Design & Outsourcing发布的2022年全球医疗器械企业百强榜,有两家中国企业成功入榜,分别是位列第32位的迈瑞医疗和位列第77位的微创医疗。2022年首届世界知识产权组织“全球奖”颁发给了5家创新活跃的中小企业,其中包含中国医疗器械企业苏州瑞派宁,展现了中国医疗器械企业在国际竞争环境下的创新趋势。
产业综合发展指数稳定提升
“十四五”开局势头良好,产业综合发展社会公众满意度处于高位。南方所研究发布:2021年,中国医疗器械产业综合发展指数(NFI指数)为336点,比“十三五”期末提高了76.5点。其中,规模效益子指数稍有下滑,为50.2点,较2020年降低了3.6点;创新发展子指数继续保持快速上升势头,为148.5点,较2020年提高46.6点;产业生态子指数持平,为5.3点,提高0.2点;国际竞争子指数稳定上升,为131.8点,较2020年提高33.2点。南方所研究报告(中国药品监督管理研究会立项课题)显示,我国医疗器械安全公众满意度处在高位水平,表明终端使用环节对医疗器械产品安全反馈总体良好。
加强监管工作的建议
一是进一步深化“放管服”改革。加大政策引导优化服务力度。对于新发布的法规、标准、导则设置合理的过渡期,实施前强化宣贯,加强事中指导,监测执行情况,及时优化调整。充分发挥国家药监局医疗器械技术审评检查两个分中心审评审批创新作用,探索试行注册审评资料预审核交流制度,在产品申报前就临床应用、关键技术或者原材料验证确认等方面建立沟通路径。
二是加强监管方式创新。加强医疗器械科学监管与监管科学研究,加快科技成果转移转化,强化政策法规执行情况及实施效果的调查和评估。加强监管信息化建设,建立统一的基础数据公共数据池,构建全国一体化在线监管数据共享平台,实现监管全链条、产品全生命周期监管数据实时共享和有效利用。加强网络监测能力建设,提高基层监管人员对网售违法违规行为的处置能力,深挖违法违规线索,力争多办大案要案,提高监管的震慑作用。
三是继续加强政策法规与产业经济研究。坚持良法出善治,坚持监管立法的系统性、整体性、协同性、时效性。继续提高公众对政策的认知和理解,强化法规标准源头治理。加强医疗器械产业区域分布、技术领域特点及产业链研究,提高统筹监管资源配置与产业布局的科学性。做好真实世界数据应用研究,继续推动相关的准则和要求的制定,推动真实世界数据在产品注册和监管中的应用。
四是加强跨部门沟通协调。加强跨部门有关产品命名、管理分类和编码等政策协商合作,做到有章可依、有序可循,发现问题,及时调整。加强跨部门违法违规线索信息共享和联合检查执法,加强案件查办。建立检验资源共享机制,对友邻部门提供医疗器械属性鉴定、产品质量检验等方面技术支持。
五是拓展和深化国际交流合作。积极参与国际监管交流与合作,协同多边统一的审评、检查标准和结果认可机制,推动多边区域特别是“一带一路”沿线国家和地区的监管趋同。鼓励企业参与国际标准、监管法规的政策制定,共同加强国内外法规对比研究;提升中国医疗器械标准、工具、方法国际认可度、影响力及话语权。
六是多措并举推进社会共治。鼓励行业协会与头部企业开展及参与政策法规、技术规范、团体标准、推荐性标准研究与制修订工作,充分发挥行业协会与头部企业引领带头作用,加快新技术新业态的发展。推动诚信建设,引导企业依法开展生产经营活动,依法曝光违法违规典型案例,加强面向消费者的科普宣传,提高人民群众用械安全意识,提升公众科学认知能力。
下一篇:{賭馬}(香水 知识)
发表评论